 |
| Trụ sở Bộ Y tế. |

 |
| Trụ sở Bộ Y tế. |
Ngày 18/9, Công an quận 7, TPHCM tạm giữ 9 đối tượng trong băng nhóm giang hồ thực hiện việc bắt giữ 3 người trái pháp luật đánh đập đòi con nợ 1 tỷ đồng.
Theo điều tra, Nguyễn Bá Huy (SN 1988, ngụ quận 7) có quen biết với người tên Dũng (chưa rõ lai lịch) và cho người này vay số tiền 1 tỷ đồng. Sau 1 thời gian, Dũng không có tiền trả nợ nên bỏ trốn.

Tại nhiều tuyến đường ở Hà Nội, xe tải ngang nhiên dừng đỗ, bốc xếp hàng hóa kéo dài nhiều giờ, hình thành những “bến cóc” tự phát.

Vụ việc bắt cóc em bé trên phố Lộ Diêu, phường Hoài Nhơn Đông, tỉnh Gia Lai được phát thông tin từ tài khoản Facebook "Bảo Nguyên" khiến dư luận đặt câu hỏi: Tin thật - giả và động cơ là gì?

Chủ tịch ACV Vũ Thế Phiệt bị vì nhận tiền để tạo điều kiện cho nhà thầu được trúng thầu.

Công ty HJC đã sử dụng các tài khoản cá nhân để giao dịch hơn 1.300 tỷ đồng nhằm che giấu doanh thu thực tế và trốn thuế hơn 4,2 tỷ đồng.

Sau vụ ngộ độc bánh mì, hơn 90 người nhập viện, các cơ sở y tế đang phối hợp điều trị và giám sát chặt chẽ tình hình sức khỏe.

Một cô gái ở Phú Thọ bị xử phạt 7,5 triệu đồng sau khi đăng tin sai sự thật về việc Việt Nam sáp nhập các tỉnh còn 16 đơn vị, gây hoang mang dư luận.

Hỏa hoạn bùng phát tại nhà dân ở phường Việt Trì, lực lượng Cảnh sát PCCC Công an tỉnh Phú Thọ kịp thời giải cứu cụ bà 92 tuổi mắc kẹt.

Công an TP Hải Phòng vừa khởi tố, bắt tạm giam 3 nhân viên ngân hàng Agribank chi nhánh Kiến Thụy liên quan dự án nhà ở Anh Dũng IV.

Tổng số tiền các đối tượng trong hệ thống Xôi Lạc TV thu lời bất chính từ hoạt động phi pháp lên đến hàng trăm tỷ đồng.

Suốt 4 năm qua, một người con dâu ở Đắk Lắk đã lén dùng vàng giả tráo 280 chỉ vàng thật của cha mẹ chồng rồi mang đi bán.

Bộ Nội vụ khẳng định hiện chưa có đề xuất điều chỉnh lịch nghỉ lễ để kéo dài kỳ nghỉ Giỗ Tổ Hùng Vương và 30/4 – 1/5 lên 9 ngày như thông tin lan truyền.

Ngày 6/3, Cổng thông tin Phật giáo Việt Nam đăng tải thông tin cho biết, Giáo hội đã yêu cầu xác minh tư cách tu sĩ người có pháp danh Thích Nhuận Đạt.

Lúc 10h15', ngày 6/3, sà lan tự hành Thành Đạt 86 đã va chạm với nhịp giữa cầu đường sắt Ghềnh. Tuyến đường sắt Bắc - Nam đi và đến bị tê liệt.

Để bảo vệ tuyến bờ biển khu vực hai bên cửa biển Cửa Lở, tỉnh Quảng Ngãi sẽ đầu tư xây dựng tuyến kè cùng nhiều hạng mục khác trị giá gần 1.000 tỷ đồng.


Được công nhận thêm 4 di sản văn hóa phi vật thể quốc gia giúp Quảng Ngãi tôn vinh bản sắc, thúc đẩy du lịch và phát huy các giá trị truyền thống dân tộc.

Chủ tịch ACV Vũ Thế Phiệt bị vì nhận tiền để tạo điều kiện cho nhà thầu được trúng thầu.

Công an TP Hải Phòng vừa khởi tố, bắt tạm giam 3 nhân viên ngân hàng Agribank chi nhánh Kiến Thụy liên quan dự án nhà ở Anh Dũng IV.

Hỏa hoạn bùng phát tại nhà dân ở phường Việt Trì, lực lượng Cảnh sát PCCC Công an tỉnh Phú Thọ kịp thời giải cứu cụ bà 92 tuổi mắc kẹt.

Tổng số tiền các đối tượng trong hệ thống Xôi Lạc TV thu lời bất chính từ hoạt động phi pháp lên đến hàng trăm tỷ đồng.

Vụ việc bắt cóc em bé trên phố Lộ Diêu, phường Hoài Nhơn Đông, tỉnh Gia Lai được phát thông tin từ tài khoản Facebook "Bảo Nguyên" khiến dư luận đặt câu hỏi: Tin thật - giả và động cơ là gì?
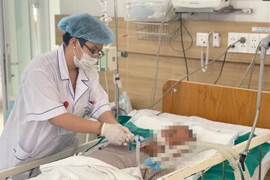
10 người ăn trưa tại Sơn La, trong đó 3 người bị ngộ độc nặng, đang được điều trị tích cực tại Bệnh viện Bạch Mai, cảnh báo nguy cơ thực phẩm không an toàn.

Một năm sau khi Thông tư 29 về dạy thêm, học thêm có hiệu lực, tình trạng dạy thêm, học thêm vẫn tồn tại, chi phí phụ huynh phải chi trả lại cao hơn trước.

Suốt 4 năm qua, một người con dâu ở Đắk Lắk đã lén dùng vàng giả tráo 280 chỉ vàng thật của cha mẹ chồng rồi mang đi bán.

Công ty HJC đã sử dụng các tài khoản cá nhân để giao dịch hơn 1.300 tỷ đồng nhằm che giấu doanh thu thực tế và trốn thuế hơn 4,2 tỷ đồng.

Liên quan đến khối tài sản của bà Trương Mỹ Lan, Thi hành án dân sự TP HCM giảm 5% giá khởi điểm đối với nhiều tài sản kê biên sau khi đấu giá không thành.

Một chiếc ô tô chở công nhân 40 chỗ bất ngờ bốc cháy dữ dội trên quốc lộ 37, đoạn gần cổng 1 Khu công nghiệp Vân Trung, phường Nếnh (tỉnh Bắc Ninh).

Trong hai ngày 4-5/3, Lễ hội chọi trâu truyền thống xã Hải Lựu (thuộc huyện sông Lô, tỉnh Vĩnh Phúc cũ, nay là tỉnh Phú Thọ) diễn ra sôi động.

Cơ quan công an Hà Nội xử phạt 5 triệu đồng một người đăng thông tin sai về lãnh đạo, nhấn mạnh việc kiểm chứng thông tin trước khi chia sẻ.

Một cô gái ở Phú Thọ bị xử phạt 7,5 triệu đồng sau khi đăng tin sai sự thật về việc Việt Nam sáp nhập các tỉnh còn 16 đơn vị, gây hoang mang dư luận.