|
| Đình chỉ lưu hành, thu hồi thuốc viên nang mềm SOS Fever® Fort - Ảnh minh họa |

 |
| Đình chỉ lưu hành, thu hồi thuốc viên nang mềm SOS Fever® Fort - Ảnh minh họa |
Ngày 10/3, Cục Quản lý Dược có Công văn số 2205/QLD-CL về việc thông báo thu hồi lô thuốc Locobile-200 (Celecoxib 200 mg). Thuốc này có tác dụng điều trị các triệu chứng thoái hóa khớp và viêm khớp dạng thấp, giảm cơn đau cấp và đau bụng kinh. Lý do thu hồi là không đạt tiêu chuẩn về chỉ tiêu đồng đều khối lượng.
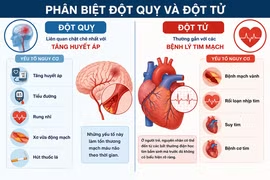

Nhiều người kỳ vọng hạt chia giúp giảm cân, tốt cho tim mạch và não bộ. Các chuyên gia cho rằng, hiệu quả còn phụ thuộc vào khả năng chuyển hóa và cách sử dụng.








Nhiều người kỳ vọng hạt chia giúp giảm cân, tốt cho tim mạch và não bộ. Các chuyên gia cho rằng, hiệu quả còn phụ thuộc vào khả năng chuyển hóa và cách sử dụng.

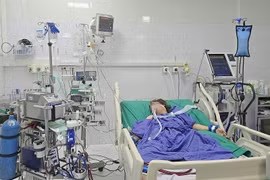
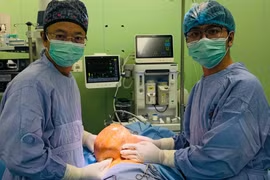

Sau hai lần đối mặt với căn bệnh u lympho Burkitt nguy hiểm, một bé trai 7 tuổi ở Hải Phòng đã hồi phục ngoạn mục nhờ được ghép tế bào gốc tạo máu đồng loài tại Bệnh viện Nhi Trung ương.


Nhiều loại trái cây ngọt, nước ép hay kem lạnh được xem là “cứu tinh” ngày nắng nóng, nhưng lại có thể làm tăng các cơn bốc hỏa ở phụ nữ tiền mãn kinh.