 |
| Vaccine Novavax đã được thử nghiệm rộng rãi, nhưng vẫn chưa được cấp phép và tung ra thị trường. Ảnh: AP. |
 |
| Vaccine Novavax đã được thử nghiệm rộng rãi, nhưng vẫn chưa được cấp phép và tung ra thị trường. Ảnh: AP. |
Thông tin từ Bộ Y tế, quá trình đàm phán hai bên thống nhất khi vaccine về tới Việt Nam sẽ ưu tiên tiêm cho những người Trung Quốc đang làm việc tại Việt Nam, người có nhu cầu đi học tập và công tác tại Trung Quốc và cư dân ở khu vực biên giới.
Bộ Y tế vừa có quyết định phân bổ triệu liều vaccine AstraZeneca cho 63 tỉnh thành, 23 đơn vị trực thuộc và lực lượng công an, quân đội. Nguồn vaccine này do cơ chế COVAX viện trợ và VNVC nhập khẩu.
28 tỉnh miền Bắc tiếp nhận gần 1,1 triệu liều vaccine, bằng số lượng phân bổ cho 20 tỉnh phía Nam.

Một số thực phẩm quen thuộc là nguồn dưỡng chất dồi dào, giúp người trung niên và cao tuổi tăng sức đề kháng, cải thiện tiêu hóa, duy trì năng lượng.

Một người hiến tinh trùng mang đột biến gene TP53 đã truyền gene nguy hiểm cho hàng trăm trẻ ở 14 nước châu Âu, đặt ra câu hỏi về quy trình kiểm tra an toàn.

Nam thanh niên 32 tuổi ngộ độc tetrodotoxin từ cá nóc được cứu sống nhờ cấp cứu kịp thời.

Người đàn ông viêm tụy cấp nặng do lạm dụng rượu, cảnh báo hậu quả nghiêm trọng nếu không phát hiện và điều trị kịp thời.
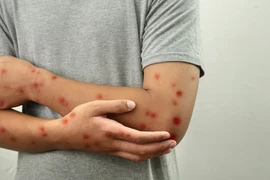
Bệnh nhân nam sinh năm 1992 ở Trảng Bom nhiễm đậu mùa khỉ, đã ổn định sau điều trị. Lực lượng y tế truy vết để ngăn chặn dịch lây lan.

Một bệnh nhân bị ong vò vẽ đốt đã thoát khỏi nguy hiểm nhờ cấp cứu kịp thời, cảnh báo không tự ý xử lý tại nhà khi gặp phản ứng phản vệ.
Bệnh não mô cầu cực kỳ nguy hiểm vì có thể diễn tiến nặng và gây tử vong chỉ trong vòng 24 giờ kể từ khi có triệu chứng như sốt cao, đau đầu dữ dội, mệt mỏi...

Một số thức uống màu đỏ giàu chất chống oxy hóa được chứng minh giúp giảm cholesterol LDL, hỗ trợ tim mạch khỏe mạnh khi được bổ sung điều độ.





Một số thức uống màu đỏ giàu chất chống oxy hóa được chứng minh giúp giảm cholesterol LDL, hỗ trợ tim mạch khỏe mạnh khi được bổ sung điều độ.

Người đàn ông viêm tụy cấp nặng do lạm dụng rượu, cảnh báo hậu quả nghiêm trọng nếu không phát hiện và điều trị kịp thời.

Nam thanh niên 32 tuổi ngộ độc tetrodotoxin từ cá nóc được cứu sống nhờ cấp cứu kịp thời.

Một số thực phẩm quen thuộc là nguồn dưỡng chất dồi dào, giúp người trung niên và cao tuổi tăng sức đề kháng, cải thiện tiêu hóa, duy trì năng lượng.

Bệnh não mô cầu cực kỳ nguy hiểm vì có thể diễn tiến nặng và gây tử vong chỉ trong vòng 24 giờ kể từ khi có triệu chứng như sốt cao, đau đầu dữ dội, mệt mỏi...

Bệnh nhân nam sinh năm 1992 ở Trảng Bom nhiễm đậu mùa khỉ, đã ổn định sau điều trị. Lực lượng y tế truy vết để ngăn chặn dịch lây lan.

Một người hiến tinh trùng mang đột biến gene TP53 đã truyền gene nguy hiểm cho hàng trăm trẻ ở 14 nước châu Âu, đặt ra câu hỏi về quy trình kiểm tra an toàn.

Một bệnh nhân bị ong vò vẽ đốt đã thoát khỏi nguy hiểm nhờ cấp cứu kịp thời, cảnh báo không tự ý xử lý tại nhà khi gặp phản ứng phản vệ.

Chân giò heo, món thịt mùa đông giàu collagen, được xem như ‘vũ khí’ dưỡng da, giúp phụ nữ giữ làn da săn chắc, mịn màng và trẻ trung tự nhiên.

Hoạt động nhảy dây giúp cho cơ thể được vận động toàn diện, tăng khả năng đốt cháy calo nhiều hơn.
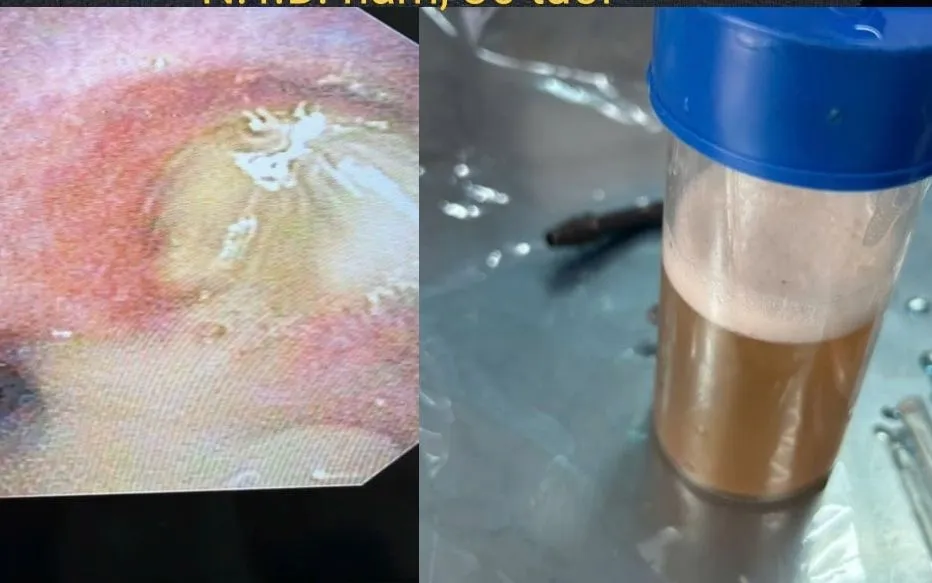
Bệnh viện Đa khoa tỉnh Quảng Ninh ghi nhận hai ca viêm phổi nặng do sặc dầu, cảnh báo nguy cơ suy hô hấp và tử vong nếu không được xử trí kịp thời.

Sản phụ 49 tuổi đã vượt qua nhiều thử thách để chào đón bé yêu đầu lòng bằng phương pháp sinh mổ.
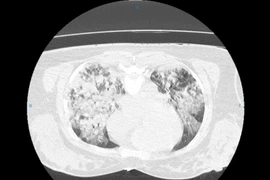
Sau nhiều ngày cấp cứu, bệnh nhân bị đuối nước mặn nguy kịch được hồi phục chức năng phổi, rút ống nội khí quản và xuất viện trong tình trạng ổn định.

Bệnh nhân bị gãy xương do áo mưa cuốn vào bánh xe, cảnh báo cần cẩn trọng khi sử dụng áo mưa cánh dơi trong thời tiết xấu.
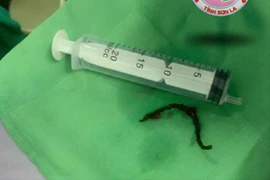
Bệnh nhân 48 tuổi được nội soi cấp cứu thành công dị vật 12 cm trong thực quản, tránh biến chứng nguy hiểm và ổn định sức khỏe sau thủ thuật.

Nhỏ nhắn nhưng giàu dinh dưỡng, quất hồng bì giúp bảo vệ tim mạch, tăng sức đề kháng và dưỡng da mịn màng, ngăn lão hóa từ bên trong.

Bệnh nhi 12 tuổi bị toan chuyển hóa do toan hóa ống thận type I, nhưng điều trị kịp thời giúp trẻ phục hồi hoàn toàn và phát triển bình thường.

Bệnh nhân 32 tuổi bị chấn thương mắt phức tạp sau tai nạn lao động vừa được Khoa Mắt, Bệnh viện Trung ương Thái Nguyên phẫu thuật cấp cứu thành công.
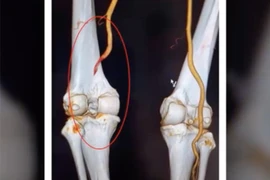
Bệnh nhân 65 tuổi ở Phú Thọ bị bò đá đứt mạch máu khoeo, được bác sĩ tái lập tuần hoàn, giữ lại chi thể.

Mùa đông dễ khiến cơ thể mệt mỏi, tuần hoàn máu kém, những thói quen uống ấm hằng ngày giúp giữ tim khỏe, cơ thể tràn đầy năng lượng.