Cục Quản lý Dược (Bộ Y tế) vừa ban hành Công văn số 5138/QLD-MP ngày 15/12/2025 về việc tăng cường các biện pháp đấu tranh ngăn chặn, đẩy lùi tình trạng buôn lậu, gian lận thương mại và hàng giả trong lĩnh vực dược, mỹ phẩm.
Theo Cục Quản lý Dược, thực hiện chỉ đạo của Bộ Y tế tại Công văn số 8660/BYT-QLD ngày 10/12/2025 về việc tăng cường các biện pháp đấu tranh ngăn chặn, đẩy lùi tình trạng buôn lậu, gian lận thương mại và hàng giả trong lĩnh vực dược, mỹ phẩm trong những tháng cuối năm 2025, nhất là dịp trước, trong và sau Tết Nguyên đán Bính Ngọ 2026, bảo đảm nhân dân đón Tết an toàn, lành mạnh. Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố khẩn trương phối hợp với Ban Chỉ đạo 389 tỉnh, thành phố và các lực lượng chức năng trên địa bàn (Quản lý thị trường, Công an, Hải quan…) triển khai đợt cao điểm kiểm tra việc chấp hành các quy định của pháp luật trong lĩnh vực y tế đối với các cơ sở đăng ký thuốc, cơ sở công bố, cơ sở sản xuất, kinh doanh dược, mỹ phẩm từ ngày 15/12/2025 đến ngày 31/3/2026.
Nội dung kiểm tra bao gồm tính pháp lý của cơ sở sản xuất, kinh doanh (Giấy chứng nhận đủ điều kiện kinh doanh và việc duy trì điều kiện kinh doanh), tính hợp pháp của sản phẩm sản xuất kinh doanh (Giấy đăng ký lưu hành thuốc/số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm); nguồn gốc xuất xứ sản phẩm; chất lượng sản phẩm; ghi nhãn sản phẩm…

Trong đó, đối với thuốc chú trọng Giấy chứng nhận đủ điều kiện kinh doanh dược; việc duy trì GPs; số đăng ký lưu hành/giấy phép nhập khẩu, nguồn gốc, xuất xứ, hóa đơn, chứng từ mua bán; hạn dùng; mua bán theo đơn. Còn đối với mỹ phẩm chú trọng Giấy chứng nhận đủ điều kiện sản xuất mỹ phẩm; hoạt động công bố sản phẩm mỹ phẩm và cung cấp hồ sơ thông tin sản phẩm (Product Information File - PIF), sự phù hợp thông tin công bố sản phẩm và sản phẩm sản xuất, nhập khẩu; việc ghi nhãn sản phẩm (thành phần, tính năng, công dụng), hoạt động quảng cáo mỹ phẩm; nguồn gốc, xuất xứ, hóa đơn, chứng từ mua bán, hồ sơ nhập khẩu (đối với các sản phẩm nhập khẩu) ...
Cùng với đó, tăng cường rà soát, kiểm tra hoạt động kinh doanh thuốc, mỹ phẩm trên sàn thương mại điện tử (Shopee, Lazada, Tiki, TikTok Shop…) và mạng xã hội (Facebook, Instagram, TikTok, YouTube...). Trường hợp phát hiện kinh doanh các sản phẩm không được phép cấp phép lưu hành (đối với thuốc) hoặc không được cơ quan chức năng tiếp nhận công bố sản phẩm (đối với mỹ phẩm); kinh doanh các sản phẩm không được phép kinh doanh theo hình thức thương mại điện tử; kinh doanh các sản phẩm đã có thông báo thu hồi, tiêu hủy của các cơ quan chức năng; quảng cáo các sản phẩm vi phạm quy định về quảng cáo, cần kịp thời xử lý và phản ánh về Bộ Công Thương; Bộ Văn hóa.
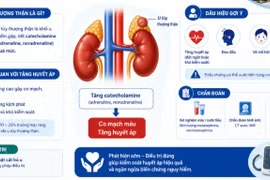
Ảnh minh họa/Internet
Kiên quyết xử lý các tổ chức, cá nhân vi phạm theo quy định của pháp luật, bảo đảm không có vùng cấm, không có ngoại lệ. Chuyển hồ sơ tới cơ quan điều tra để xử lý hình sự theo quy định trong trường hợp có dấu hiệu tội phạm (giá trị hàng hóa lớn, gây hậu quả nghiêm trọng, sai phạm có tổ chức, tái phạm…)
Cục cũng yêu cầu báo cáo kết quả kiểm tra và xử lý vi phạm, cụ thể: đối với các đoàn kiểm tra và xử lý vi phạm đã hoàn thành trước ngày 25/12/2025 thì báo cáo về Cục Quản lý Dược trước ngày 31/12/2025; đối với các đoàn kiểm tra và xử lý vi phạm đã hoàn thành từ ngày 25/12/2025 đến ngày 31/3/2026 thì báo cáo về Cục Quản lý Dược trước ngày 15/4/2026.
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố phối hợp với các cơ quan chức năng trên địa bàn để khẩn trương triển khai, thực hiện bảo đảm công tác quản lý dược, mỹ phẩm được thực hiện hiệu quả, kịp thời, bảo vệ sức khỏe và quyền lợi của người tiêu dùng. Trong quá trình triển khai thực hiện, đề nghị Sở Y tế các tỉnh, thành phố kịp thời báo cáo các khó khăn vướng mắc về Cục Quản lý Dược để giải quyết.