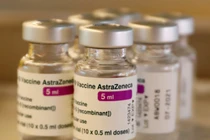
Seroquel XR chứa hoạt chất Quetiapin (dưới dạng Quetiapin fumarat) với các hàm lượng 200 mg, 300 mg, 400 mg, 50 mg. Sản phẩm này thuộc về cơ sở đăng ký thuốc là AstraZeneca Singapore Pte., Ltd. có địa chỉ tại số 10, Kallang Avenue #12-10 Aperia, Singapore 339510 - Singapore.
Cụ thể, Seroquel XR, viên nén phóng thích kéo dài, thuộc cơ sở sản xuất thuốc AstraZeneca UK Ltd. (Đ/c: Silk Road Business Park, Macclesfield, Cheshire, SK10 2NA - United Kingdom).
 |
| Ảnh minh họa |
Bên cạnh đó, Seroquel XR, Cơ sở sản xuất thuốc: AstraZeneca Pharmaceuticals LP (Đ/c: Newark, DE 19702, USA - USA), được đóng gói tại (cơ sở đóng gói: AstraZeneca Pharmaceutical Co., Ltd. Địa chỉ: Số 2, đường Huangshan, Wuxi, Jiangsu, Trung Quốc) cũng đã bị thu hồi Giấy đăng ký lưu hành thuốc tại Việt Nam.
Thuốc Seroquel XR với thành phần chính là Quetiapine, được sử dụng đơn độc hoặc kết hợp với các thuốc khác để điều trị tâm thần phân liệt và rối loạn lưỡng cực và điều trị trầm cảm.
Theo ông Nguyễn Thành Lâm, Phó Cục trưởng, Cục Quản lý Dược (Bộ Y tế), các cơ sở đăng ký thuốc tự nguyện đề nghị thu hồi giấy đăng ký lưu hành tại Việt Nam.
Thuốc trong nước được sản xuất trước ngày quyết định này có hiệu lực, thuốc nước ngoài nhập khẩu vào Việt Nam hoặc thuốc nước ngoài nhập khẩu trong trường hợp được giao hàng tại cảng đi của nước xuất khẩu trước ngày quyết định này có hiệu lực được phép lưu hành đến hết hạn dùng của thuốc.
Cơ sở đăng ký thuốc, sản xuất thuốc phải có trách nhiệm theo dõi và chịu trách nhiệm về chất lượng, an toàn, hiệu quả của thuốc trong quá trình lưu hành.