 |
| Thuốc Cefpomed-200 do công ty Dược Daphaco nhập khẩu bị thu hồi. |
| Thuốc kháng sinh Doxycycline capsules BP 100mg không đạt tiêu chuẩn chất lượng |
 |
| Thuốc Cefpomed-200 do công ty Dược Daphaco nhập khẩu bị thu hồi. |
| Thuốc kháng sinh Doxycycline capsules BP 100mg không đạt tiêu chuẩn chất lượng |
 |
| Viên nang ích mẫu Abipha. |
 |
| Sản phẩm thuốc Cefpomed-200 do công ty Dược Daphaco phân phối. |
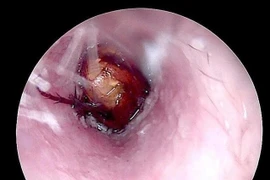
Khi phát hiện côn trùng chui vào tai, người bệnh đã đến tiệm cắt tóc để lấy nhưng không được, sau đó được người nhà đưa đến bệnh viện thăm khám.
Một người phụ nữ ở tỉnh Lâm Đồng bị rắn độc cắn, nhưng không đến bệnh viện mà tự chữa bằng thuốc dân gian dẫn đến nguy kịch.

Các chuyên gia cảnh báo tác hại của bụi mịn đối với mắt, khuyến khích người dân theo dõi chất lượng không khí và thực hiện các biện pháp bảo vệ đúng cách.

Dù giàu protein và vitamin, cá lóc cần hạn chế với người mắc bệnh gout, gan, thận hoặc dị ứng để tránh rủi ro sức khỏe.

Thay vì các phương pháp “detox” nguy hiểm, hãy duy trì thói quen uống đủ nước, ăn rau quả, ngủ đủ giấc và vận động nhẹ nhàng để giữ gìn sức khỏe lâu dài.

Bảo quản thực phẩm trong tủ lạnh không đúng cách hoặc để quá thời gian khuyến nghị, thực phẩm vẫn có thể bị nhiễm khuẩn, gây ngộ độc.

Bổ sung nước, ăn uống cân bằng thực phẩm và lối sống lành mạnh giúp gan khỏe mạnh, giảm tổn thương do rượu bia gây ra.



Bảo quản thực phẩm trong tủ lạnh không đúng cách hoặc để quá thời gian khuyến nghị, thực phẩm vẫn có thể bị nhiễm khuẩn, gây ngộ độc.


Thay vì các phương pháp “detox” nguy hiểm, hãy duy trì thói quen uống đủ nước, ăn rau quả, ngủ đủ giấc và vận động nhẹ nhàng để giữ gìn sức khỏe lâu dài.

Độ ẩm cao tạo điều kiện cho nấm mốc, vi khuẩn phát triển, gây kích ứng và làm suy yếu hệ hô hấp, dễ dẫn đến các bệnh như viêm mũi, hen suyễn...


Dù giàu protein và vitamin, cá lóc cần hạn chế với người mắc bệnh gout, gan, thận hoặc dị ứng để tránh rủi ro sức khỏe.

Bổ sung nước, ăn uống cân bằng thực phẩm và lối sống lành mạnh giúp gan khỏe mạnh, giảm tổn thương do rượu bia gây ra.


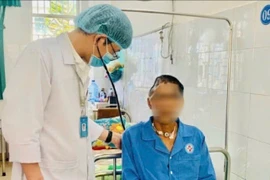
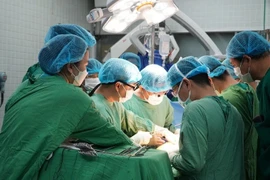
Tại Bệnh viện Da liễu Trung ương, sự phối hợp giữa bác sĩ và điều dưỡng đã giúp người bệnh vượt qua hoại tử da nặng nề, hồi phục kỳ diệu.

Một người phụ nữ ở tỉnh Lâm Đồng bị rắn độc cắn, nhưng không đến bệnh viện mà tự chữa bằng thuốc dân gian dẫn đến nguy kịch.

Khi phát hiện côn trùng chui vào tai, người bệnh đã đến tiệm cắt tóc để lấy nhưng không được, sau đó được người nhà đưa đến bệnh viện thăm khám.

Các chuyên gia cảnh báo tác hại của bụi mịn đối với mắt, khuyến khích người dân theo dõi chất lượng không khí và thực hiện các biện pháp bảo vệ đúng cách.

Sau những ngày Tết, việc lắng nghe các tín hiệu cảnh báo của cơ thể chính là bước quan trọng để bảo vệ sức khỏe lâu dài trong năm mới.