Ngày 11/8, Thứ trưởng Y tế Trương Quốc Cường vừa ký văn bản gửi UBND TP.HCM về việc sử dụng vắc xin COVID-19 Vero Cell Inactivated (Sinopharm).
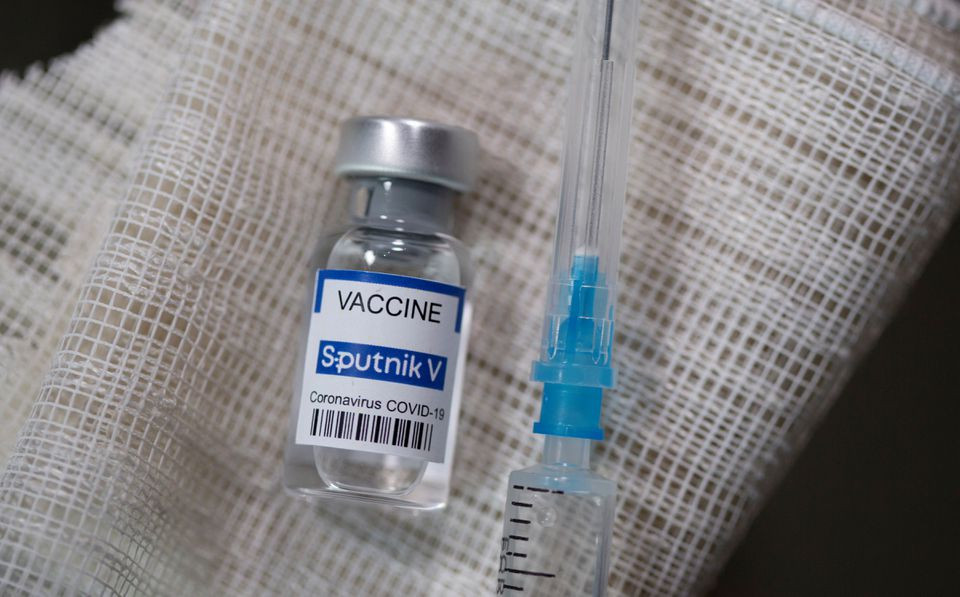
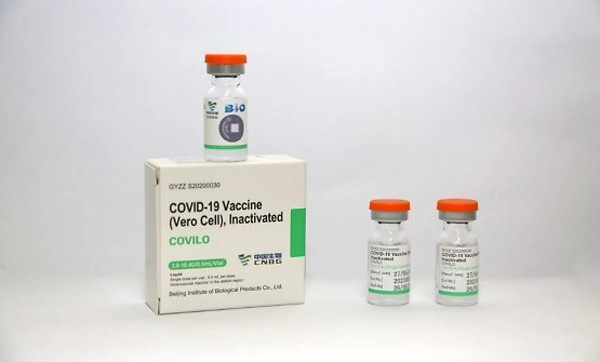
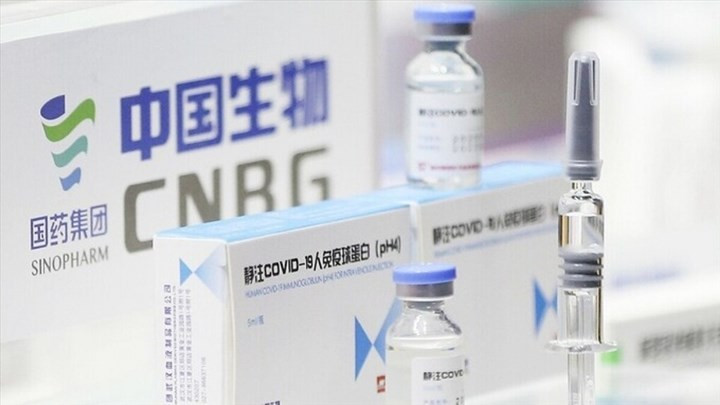
Bộ Y tế cho biết vắc xin Sinopharm do Viện Sản phẩm sinh học Bắc Kinh thuộc Tập đoàn Biotec quốc gia Trung Quốc (CNBG) sản xuất. vắc xin này đã được Tổ chức Y tế Thế giới (WHO) phê duyệt nằm trong danh sách vắc xin sử dụng khẩn cấp để phòng, chống dịch COVID-19. Sinopharm cũng được nhiều nước trên thế giới đưa vào sử dụng trong tiêm chủng.
Tại Việt Nam, từ ngày 3/6, Bộ trưởng Y tế đã phê duyệt có điều kiện vắc xin Sinopharm cho nhu cầu cấp bách phòng, chống dịch và trên cơ sở đề nghị nhập khẩu vắc xin COVID-19 của Công ty TNHH Một thành viên Dược Sài Gòn (Sapharco).
Ngày 8/7, Bộ Y tế đã đồng ý để Sapharco nhập khẩu 5 triệu liều vắc xin Sinopharm, thuộc đơn hàng số 272/ĐH-SPC-XNK đề ngày 1/7.
Ngày 31/7, Sapharco đã tiến hành thủ tục nhập khẩu thông quan tại sân bay quốc tế Tân Sơn Nhất và tiếp nhận 4 lô vắc xin với tổng số lượng một triệu liều, bảo quản tại kho của công ty.
Bộ Y tế nói rõ các lô vắc xin này đã được Viện Kiểm định Quốc gia vắc xin và Sinh phẩm y tế kiểm định chất lượng và cấp các Giấy chứng nhận xuất xưởng vắc xin, sinh phẩm y tế số 11421/VXVR-TT, 11521/VXVR-TT, 11621/VXVR-TT, 11721/VXVR-TT ngày 4/8.
Do đó, các lô vắc xin nhập khẩu này đủ điều kiện để đưa ra sử dụng. Theo quyết định phê duyệt cấp phép khẩn cấp, công ty Sapharco chịu trách nhiệm về nguồn gốc, chất lượng vắc xin nhập khẩu; đảm bảo việc bảo quản vắc xin tại các cơ sở bảo quản theo đúng quy định, tránh ảnh hưởng đến chất lượng vắc xin nhập khẩu; đồng thời bảo đảm việc sử dụng vắc xin phục vụ nhu cầu tiêm chủng theo chỉ đạo của UBND TP.HCM.