 |
| Công ty Deahwa Pharmaceutical Co., Ltd bị phạt 70 triệu đồng do sản xuất thuốc viên nang mềm Daehwa Haris không đạt tiêu chuẩn chất lượng |

 |
| Công ty Deahwa Pharmaceutical Co., Ltd bị phạt 70 triệu đồng do sản xuất thuốc viên nang mềm Daehwa Haris không đạt tiêu chuẩn chất lượng |

Gan là cơ quan thầm lặng nhưng giữ vai trò giải độc, chuyển hóa quan trọng. Một số loại trái cây quen thuộc có thể hỗ trợ bảo vệ gan và giảm nguy cơ tổn thương.


Rau khoai lang giàu vitamin, hợp chất sinh học giúp chống oxy hóa, kiểm soát đường huyết, bảo vệ gan và hỗ trợ phòng ngừa ung thư.
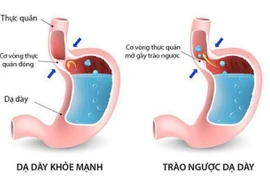
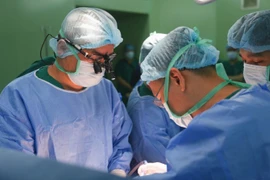
Lối sống, chế độ ăn uống và căng thẳng là những yếu tố chính gây trào ngược dạ dày. Thay đổi thói quen và khám sớm giúp giảm nguy cơ mắc bệnh nặng.

Học cách lựa chọn, sơ chế và kết hợp hải sản đúng cách để tránh ngộ độc, đảm bảo sức khỏe khi thưởng thức món ngon từ biển cả.

Thay vì lo lắng hay tìm đến những biện pháp thiếu an toàn, chị em hoàn toàn có thể áp dụng một số cách tự nhiên, lành tính dưới đây.

Sau Tết, nhiều gia đình dư bánh chưng nhưng lo bảo quản khó. Áp dụng 3 cách trữ đơn giản dưới đây giúp bánh để lâu, không mốc, không sượng mà vẫn dẻo ngon.

Các loại hạt như óc chó, hạnh nhân, hạt điều hay hướng dương chứa nhiều vitamin E, omega-3 và kẽm, giúp bảo vệ võng mạc, giảm khô mắt...







Sau Tết, nhiều gia đình dư bánh chưng nhưng lo bảo quản khó. Áp dụng 3 cách trữ đơn giản dưới đây giúp bánh để lâu, không mốc, không sượng mà vẫn dẻo ngon.


Rửa rau là bước quen thuộc nhưng nhiều thói quen tưởng sạch lại phản tác dụng, khiến rau mất dinh dưỡng, dễ nhiễm bẩn và tăng nguy cơ tồn dư hóa chất.

Thịt gà có tính ấm, khi kết hợp với cá chép hay tỏi có thể gây khó tiêu, nổi mụn hoặc nóng trong, ảnh hưởng sức khỏe và hương vị món ăn.

Các loại hạt như óc chó, hạnh nhân, hạt điều hay hướng dương chứa nhiều vitamin E, omega-3 và kẽm, giúp bảo vệ võng mạc, giảm khô mắt...

Học cách lựa chọn, sơ chế và kết hợp hải sản đúng cách để tránh ngộ độc, đảm bảo sức khỏe khi thưởng thức món ngon từ biển cả.

Thay vì lo lắng hay tìm đến những biện pháp thiếu an toàn, chị em hoàn toàn có thể áp dụng một số cách tự nhiên, lành tính dưới đây.

Gan là cơ quan thầm lặng nhưng giữ vai trò giải độc, chuyển hóa quan trọng. Một số loại trái cây quen thuộc có thể hỗ trợ bảo vệ gan và giảm nguy cơ tổn thương.



Rau khoai lang giàu vitamin, hợp chất sinh học giúp chống oxy hóa, kiểm soát đường huyết, bảo vệ gan và hỗ trợ phòng ngừa ung thư.

Lối sống, chế độ ăn uống và căng thẳng là những yếu tố chính gây trào ngược dạ dày. Thay đổi thói quen và khám sớm giúp giảm nguy cơ mắc bệnh nặng.

Một ngày không điện thoại mang đến nhiều thay đổi tích cực cho giấc ngủ, tinh thần và khả năng tập trung.

Ưu tiên thực phẩm giàu carbs phức hợp, vitamin và lợi khuẩn giúp bạn duy trì thể lực, đề kháng tốt và tận hưởng trọn vẹn chuyến đi đầu năm.

Nhịp sống chậm nơi làng quê giúp tâm hồn bình yên, giảm căng thẳng, gắn kết con người và thiên nhiên trong từng khoảnh khắc giản dị.

Nhiều gia đình cho rau vào tủ lạnh ngay sau khi mua nhưng cách này khiến rau nhanh hỏng. Chỉ cần thêm một tờ giấy ăn đúng chỗ, rau có thể giữ độ tươi hàng tuần.

Tạm dừng cà phê trong một tuần, nhiều người trải qua cảm giác uể oải ban đầu nhưng dần nhận ra giấc ngủ và tinh thần ổn định hơn.