 |
| Những viên thuốc được giới thiệu là hỗ trợ chữa bệnh ung thư làm từ than tre. |
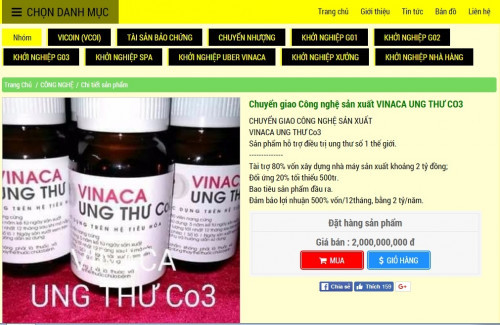 |
| Trên website chính thức loại thuốc này được quảng bá chữa bệnh ung thư số 1 thế giới. Ảnh chụp màn hình. |
 |
| Những viên thuốc được giới thiệu là hỗ trợ chữa bệnh ung thư làm từ than tre. |
 |
| Trên website chính thức loại thuốc này được quảng bá chữa bệnh ung thư số 1 thế giới. Ảnh chụp màn hình. |
Công ty dược phẩm Aurobindo có chi nhánh tại Mỹ đã cho thu hồi 47.000 hộp thuốc trống trầm cảm Venlafaxine Hydrochloride dạng viên con nhộng loại 37,5mg tại thịt trường Mỹ.
Nói về lý do thu hồi thuốc, Aurobindo cho biết một số không đạt quy chuẩn công ty, một số khác thì thuốc trong hộp bị vỡ, chảy hoặc vón cục.
| Sản phẩm thuốc tiêm Testosterone Cypionate của công ty Dược Sun Pharma. Ảnh: TheHindubusinessline. |

Sau những ngày Tết, việc lắng nghe các tín hiệu cảnh báo của cơ thể chính là bước quan trọng để bảo vệ sức khỏe lâu dài trong năm mới.

Các chuyên gia cảnh báo tác hại của bụi mịn đối với mắt, khuyến khích người dân theo dõi chất lượng không khí và thực hiện các biện pháp bảo vệ đúng cách.

Hạt macca giúp giảm cholesterol, hỗ trợ hệ tiêu hóa, làm đẹp da và tóc, đồng thời tăng cường sức khỏe xương và kiểm soát đường huyết.

Chế độ ăn ngày Tết thường quá nhiều đạm, chất béo nhưng lại thiếu hụt chất xơ từ rau xanh khiến nhiều bệnh lý chuyển hóa thường gặp sau Tết.

Trữ nem rán đúng cách giúp duy trì chất lượng và an toàn thực phẩm, tránh nguy cơ nhiễm khuẩn, mất dinh dưỡng.

Một số thói quen buổi giúp não bộ hoạt động hiệu quả, ngăn ngừa lão hóa, tăng cường tập trung và tinh thần sảng khoái để khởi đầu ngày mới.

Khám phá 5 món salad ngon, bổ dưỡng giúp thanh lọc cơ thể, giảm mỡ và lấy lại vóc dáng sau kỳ nghỉ Tết hiệu quả, an toàn.
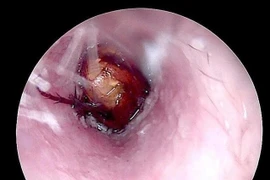
Khi phát hiện côn trùng chui vào tai, người bệnh đã đến tiệm cắt tóc để lấy nhưng không được, sau đó được người nhà đưa đến bệnh viện thăm khám.

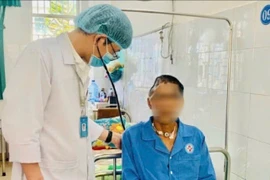

Tại Bệnh viện Da liễu Trung ương, sự phối hợp giữa bác sĩ và điều dưỡng đã giúp người bệnh vượt qua hoại tử da nặng nề, hồi phục kỳ diệu.
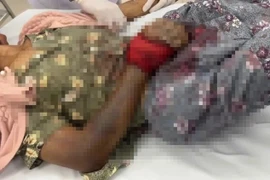
Một người phụ nữ ở tỉnh Lâm Đồng bị rắn độc cắn, nhưng không đến bệnh viện mà tự chữa bằng thuốc dân gian dẫn đến nguy kịch.

Khi phát hiện côn trùng chui vào tai, người bệnh đã đến tiệm cắt tóc để lấy nhưng không được, sau đó được người nhà đưa đến bệnh viện thăm khám.

Các chuyên gia cảnh báo tác hại của bụi mịn đối với mắt, khuyến khích người dân theo dõi chất lượng không khí và thực hiện các biện pháp bảo vệ đúng cách.
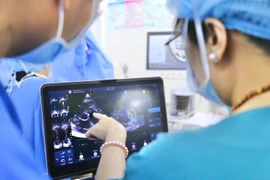
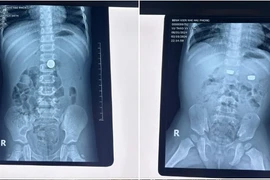

Sau những ngày Tết, việc lắng nghe các tín hiệu cảnh báo của cơ thể chính là bước quan trọng để bảo vệ sức khỏe lâu dài trong năm mới.

Chỉ vài thói quen nhỏ trước khi ngủ có thể giúp mái tóc giảm xơ rối, giữ độ ẩm tự nhiên và mềm mượt hơn khi thức dậy mà không cần tốn nhiều công chăm sóc.

Hạt macca giúp giảm cholesterol, hỗ trợ hệ tiêu hóa, làm đẹp da và tóc, đồng thời tăng cường sức khỏe xương và kiểm soát đường huyết.

Tiết trời nồm ẩm, mưa phùn đầu xuân khiến nguy cơ cảm cúm, bệnh hô hấp gia tăng. Giữ ấm, ăn uống hợp lý và sinh hoạt khoa học giúp bảo vệ sức khỏe hiệu quả.

Chế độ ăn ngày Tết thường quá nhiều đạm, chất béo nhưng lại thiếu hụt chất xơ từ rau xanh khiến nhiều bệnh lý chuyển hóa thường gặp sau Tết.

Một số thói quen buổi giúp não bộ hoạt động hiệu quả, ngăn ngừa lão hóa, tăng cường tập trung và tinh thần sảng khoái để khởi đầu ngày mới.




Trữ nem rán đúng cách giúp duy trì chất lượng và an toàn thực phẩm, tránh nguy cơ nhiễm khuẩn, mất dinh dưỡng.

Khám phá 5 món salad ngon, bổ dưỡng giúp thanh lọc cơ thể, giảm mỡ và lấy lại vóc dáng sau kỳ nghỉ Tết hiệu quả, an toàn.
